
- Autor Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:40.
- E modifikuara e fundit 2025-01-22 17:10.
Klorin izotopi me 18 neutrone ka një bollëk prej 0,7577 dhe një numër masiv prej 35 amu. Për të llogaritur mesatare masën atomike, shumëzojeni thyesën me numrin masiv për secilën izotopi , pastaj shtoni ato së bashku.
Në mënyrë të ngjashme, sa është mesatarja e ponderuar e të gjithë izotopeve të një elementi?
Duke përdorur masat e ndryshme izotopet dhe sa e bollshme secila izotopi është, ne mund të gjejmë mesatare masa e atomeve të një element . Masa atomike e një element eshte mesatare e ponderuar masa e atomeve në një mostër natyrale të element . Masa atomike zakonisht raportohet në njësitë e masës atomike.
çfarë ka një masë prej 1 amu? Një njësi e masës atomike (e simbolizuar AMU ose amu) përcaktohet saktësisht si 1/12 e masës së një atomi të karbonit-12. Atomi i karbonit-12 (C-12) ka gjashtë protonet dhe gjashtë neutronet në bërthamën e saj. Në terma të pasaktë, një AMU është mesatarja e proton masa e pushimit dhe neutron masë pushimi.
Së dyti, si e llogaritni përqindjen e bollëkut duke përdorur masën atomike?
Ndryshoni secilën për qind bollëk në formë dhjetore duke e pjesëtuar me 100. Shumëzojeni këtë vlerë me masë atomike të atij izotopi. Shtoni së bashku për çdo izotop për të marrë mesataren masë atomike.
Cili është ndryshimi midis masës atomike dhe peshës atomike?
Masa atomike (ma) eshte masë i nje atom . Një beqare atom ka një numër të caktuar të protoneve dhe neutroneve, kështu që masë është e paqartë (nuk do të ndryshojë) dhe është shuma e numrit të protoneve dhe neutroneve në atom . Pesha atomike është një mesatare e ponderuar e masë nga të gjitha atomet të një elementi, bazuar në bollëkun e izotopeve.
Recommended:
Si e interpretoni mesataren e ponderuar?

Përmbledhje. Mesatarja e ponderuar: Një mesatare ku disa vlera kontribuojnë më shumë se të tjerat. Kur peshat shtohen në 1: thjesht shumëzojeni secilën peshë me vlerën që përputhet dhe përmblidhni të gjitha. Përndryshe, shumëzojeni secilën peshë w me vlerën e saj përputhëse x, mblidhni të gjitha dhe pjesëtojeni me shumën e peshave: Mesatarja e ponderuar = ΣwxΣw
Si e gjeni mesataren dhe qendrën e një trekëndëshi?

Për të gjetur qendrën e një trekëndëshi, është më e lehtë të vizatoni të tre medianat dhe të kërkoni pikën e tyre të kryqëzimit. Për të vizatuar mesataren e një trekëndëshi, fillimisht gjeni mesin e njërës anë të trekëndëshit. Vizatoni një segment të vijës që lidh këtë pikë me kulmin e kundërt
Si të krijoni një mesatare të ponderuar në një tabelë kryesore?

Mesatarja e ponderuar në një tabelë kryesore Klikoni shigjetën poshtë pranë fjalës PivotTable në anën e majtë të shiritit të veglave të PivotTable. Zgjidhni Formulat | Fushat e llogaritura. Në kutinë Emri, vendosni një emër për fushën tuaj të re. Në kutinë Formula, vendosni formulën që dëshironi të përdoret për mesataren tuaj të ponderuar, si p.sh. =WeightedValue/Weight. Klikoni OK
Si e gjeni mesataren në një grafik?
Për të gjetur mesataren, shtoni numrat dhe pjesëtojeni shumën me numrin e shtesave
Si e gjeni mesataren dhe mesataren në tabelë?
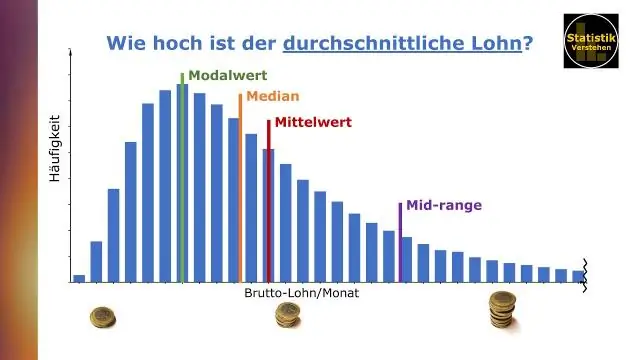
Komunikimi i të dhënave me Tableau nga Ben Jones Mesatarja (ose mesatarja) përcaktohet duke mbledhur të gjitha vlerat në një grup të dhënash dhe duke pjesëtuar me numrin e vlerave. Mediana është vlera e mesme në një grup të dhënash në të cilin vlerat janë vendosur sipas madhësisë
