
- Autor Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:40.
- E modifikuara e fundit 2025-01-22 17:10.
Mund të ketë dy elektrone në një maksimumi orbital . Nënniveli s ka vetëm një orbitale , pra mund të përmbajë 2 elektrone maksimumi . Nënniveli p ka 3 orbitalet , pra mund të përmbajë 6 elektrone maksimumi . Niveli i dyfishtë ka 5 orbitalet , pra mund të përmbajë 10 elektrone maksimumi.
Lidhur me këtë, sa është numri maksimal i orbitaleve në n 3?
| Orbitalet dhe Kapaciteti elektronik i Nivelet e Energjisë së Katër Parimit të Parë | ||
|---|---|---|
| Niveli kryesor i energjisë (n) | Lloji i nënnivelit | Numri maksimal i elektroneve (2n2) |
| 2 | fq | 8 |
| 3 | s | 18 |
| fq | ||
Për më tepër, cili është numri maksimal i elektroneve 5d? Numri maksimal i orbitaleve në një nivel energjie (n2)
| Niveli kryesor i energjisë (n) | nënnivele | elektronet totale |
|---|---|---|
| 2 | 2s 2p | 8 |
| 3 | 3s 3p 3d | 18 |
| 4 | 4s 4p 4d 4f | 32 |
| 5 | 5s 5p 5d 5f 5g | 50 |
Këtu, sa është numri maksimal i orbitaleve me N 4?
(a) Kur = 2, janë katër orbitalet (një 2s orbitale , dhe tre orbitalet etiketuar2p). Këto katër orbitalet mund përmban tetë elektrone. Përsëri, secili orbitale mban dy elektrone, pra 50 elektrone mund përshtatet me këtë guaskë. Nëse një guaskë përmban një maksimale prej 32 elektroneve, sa është kuanti kryesor numri , ?
Si e përcaktoni numrin e orbitaleve në një nënshell?
Të numri i orbitaleve në një guaskë është katrori i kuantit kryesor numri : 12 =1, 22 = 4, 32 = 9. Ka një orbitale në një shek nënshell (l = 0), tre orbitalet në një fq nënshell (l = 1) dhe pesë orbitalet në një d nënshell (l = 2). Të numri i orbitaleve ne nje nënshell është pra 2(l) +1.
Recommended:
Cili është numri natyror dhe numri i plotë me shembull?
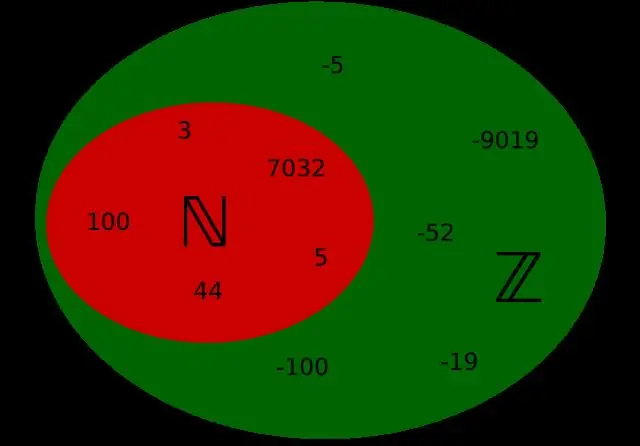
Numrat natyrorë janë të gjithë numrat 1, 2, 3, 4… Ata janë numrat që zakonisht numëroni dhe do të vazhdojnë në pafundësi. Numrat e plotë janë të gjithë numra natyrorë duke përfshirë 0 p.sh. 0, 1, 2, 3, 4… Numrat e plotë përfshijnë të gjithë numrat e plotë dhe homologun e tyre negativ p.sh.
Cili është rendi i rritjes së energjisë së orbitaleve?

Orbitalet sipas rendit të rritjes së energjisë:1s, 2s, 2p, 3s, 3p, 3d, 4s, 4p, 4d, 4f, 5s, 5p, 5d, 5f, 6s, 6p, 6d,6f, etj
Cili është numri masiv dhe numri atomik?

Numri masiv (i përfaqësuar me shkronjën A) përcaktohet si numri i përgjithshëm i protoneve dhe neutroneve në një atom. Konsideroni tabelën më poshtë, e cila tregon të dhëna nga gjashtë elementët e parë të tabelës periodike. Konsideroni elementin helium. Numri i tij atomik është 2, pra ka dy protone në bërthamën e tij
Cili është numri natyror dhe numri real?

Llojet kryesore): Numrat numërues {1, 2, 3,} zakonisht quhen numra natyrorë; megjithatë, përkufizimet e tjera përfshijnë 0, kështu që numrat e plotë jo negativë {0, 1, 2, 3,} quhen gjithashtu numra natyrorë. Numrat natyrorë duke përfshirë 0 quhen edhe numra të plotë.): Numrat realë që nuk janë racionalë
Cili është numri atomik dhe numri masiv i këtij atomi?

Numri i tij atomik është 2, pra ka dy protone në bërthamën e tij. Bërthama e saj përmban gjithashtu dy neutrone. Meqenëse 2+2=4, ne e dimë se numri masiv i atomit të heliumit është 4. Numri i masës. Emri i beriliumit Simboli Bëhu numër atomik (Z) 4 protone 4 neutrone 5
