
Përmbajtje:
- Autor Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:40.
- E modifikuara e fundit 2025-06-01 05:06.
Llogaritja e pH-së së tretësirave të kripës
- masa NaF = 20,0 g.
- masa molare NaF = 41,99 g/mol.
- vëllimi zgjidhje = 0,500 L.
- e F - = 1.4 × 10 −11
Në mënyrë të ngjashme, si e gjeni pH-në e një solucioni të kripës?
çift i konjuguar acid-bazë. Kripërat mund të jetë acid, neutral ose bazë. Kripërat që formohen nga një acid i fortë dhe një bazë e dobët janë acide kripërat , si kloruri i amonit (NH4Cl).
Gjithashtu, sa është pH e Na? pH e acideve dhe bazave të zakonshme
| Baza | Emri | 1 mm |
|---|---|---|
| Sr(OH)2 | hidroksid stroncium | 11.27 |
| NaOH | hidroksid natriumi | 10.98 |
| KOH | hidroksid kaliumi (potasë kaustike) | 10.98 |
| Na2SiO3 | metasilikat natriumi | 11.00 |
Në mënyrë të ngjashme, si e gjeni pH-në e një tretësire?
te llogaritni pH të një ujore zgjidhje ju duhet të njohin përqendrimi i jonit të hidroniumit në mol për litër (molaritet). Të pH pastaj llogaritet duke përdorur shprehjen: pH = - log [H3O+].
Sa është pH e ujit të kripur?
Të pranuarit pH nivel në një bazë ujë i kripur sistemi është midis 7.6 dhe 8.4, por rezervuarët e shkëmbinjve janë më të ndjeshëm, dhe për këtë arsye duhet të mbahen në skajin më të lartë të pH shkallë, 8.0 deri në 8.4.
Recommended:
Si të llogarisni rënien e mundshme në një qark?
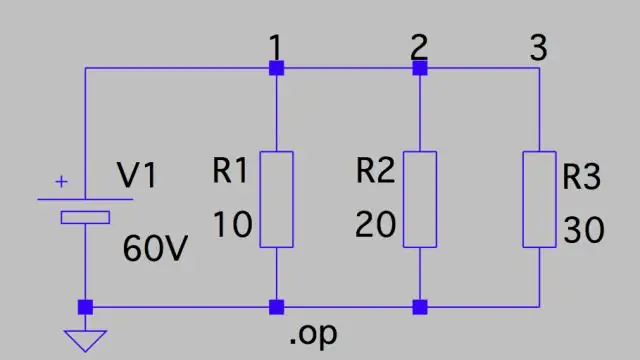
Rënia e tensionit: Qarku paralel Kjo do të thotë që rënia e tensionit në secilin është vetëm tensioni total i qarkut pjesëtuar me numrin e rezistorëve në qark, ose 24 V/3 = 8 V
Si të llogarisni energjinë e një valë elektromagnetike?

Energjia e bartur nga çdo valë është proporcionale me amplituda e saj në katror. Për valët elektromagnetike, kjo do të thotë intensiteti mund të shprehet si Iave=cϵ0E202 I ave = c ϵ 0 E 0 2 2, ku Iave është intensiteti mesatar në W/m2 dhe E0 është forca maksimale e fushës elektrike e një vale sinusoidale të vazhdueshme
Si të llogarisni peshën dhe ekuilibrin e një avioni?

Shtoni të gjitha momentet për të gjetur momentin total. Pjesëtoni momentin total me peshën bruto për të gjetur qendrën e gravitetit. Gjeni peshën totale dhe qendrën e gravitetit në grafikun e kufijve të qendrës së gravitetit në POH të avionit tuaj për të përcaktuar nëse avioni është brenda kufijve të lejueshëm
Si të llogarisni peshën e një topi?

Me një shikim Për të përcaktuar vëllimin e një sfere, duhet të merrni diametrin në fuqinë 3 dhe ta shumëzoni atë në Pi si dhe 1/6. Pesha e një objekti llogaritet duke shumëzuar vëllimin me densitetin e materialit
A është përzierja e kripës dhe piperit një veti fizike apo kimike?

Për shembull, përzierja e kripës dhe piperit krijon një substancë të re pa ndryshuar përbërjen kimike të asnjërit komponent. Ato janë gjithashtu ndryshime fizike sepse nuk ndryshojnë natyrën e substancës
