
- Autor Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:40.
- E modifikuara e fundit 2025-06-01 05:06.
Për shkak të pranisë së çifteve të vetme të elektroneve, hidridet të këtyre elementeve janë bazë (bazat Lewis) në natyrë. Të bazueshmëria zvogëlohet me madhësinë e atomit qendror për shkak të difuzionit të elektroneve në vëllim të madh d.m.th poshtë grupit , pasi madhësia e elementeve rrit densitetin e elektronit në element zvogëlohet.
Këtu, pse bazueshmëria e oksideve rritet në grup?
Aftësia e një atomi "për të pranuar një elektron" zvogëlohet në grup prandaj rritet tendenca e elementeve për të qenë baza të mira Lewis (kujtojmë se një bazë Lewis është një dhurues i çiftit elektron). Kështu ulja e afinitetit të elektroneve poshtë grupit do të thotë që elementët dhurojnë lehtësisht një elektron në vend që t'i pranojnë ato.
E dini gjithashtu, çfarë ndodh me karakterin bazë të oksideve në grup dhe pse? Acid karakteri i oksideve zvogëlohet poshtë grupit : Acidi karakter të oksidet "zvogëlohet poshtë grupit " sepse elektronegativiteti ulet poshtë grupit . Elektronegativiteti është vetia e elementit për të tërhequr çifte elektronike. Kur metali është më elektropozitiv, ai ka më shumë oksid bazë në natyrës.
Njerëzit pyesin gjithashtu, pse qëndrueshmëria e hidrideve zvogëlohet në grup?
Të qëndrueshmëria e hidrideve zvogëlohet nga amoniaku tek bismutina. Kjo është për shkak se atomi qendror E rritet në madhësi poshtë grupit . Me rritjen e madhësisë së atomit qendror, lidhja E - H bëhet më e dobët. ku E është azoti, fosfori, arseniku, antimoni, bismuti.
Pse karakteri bazë zvogëlohet gjatë një periudhe?
Në lëvizje përgjatë një periudhe , tendenca për të humbur elektrone zvogëlohet dhe kështu, metali karakteri zvogëlohet . Kështu mund të thuhet, përgjatë një periudhe nga e majta në të djathtë karakteri bazë zvogëlohet ndërsa në lëvizje poshtë, karakteri bazë rritet për shkak të rritjes së metaleve karakter.
Recommended:
Pse bazueshmëria zvogëlohet me madhësinë?

Thelbësia zvogëlohet kur dikush zbret në grup në një tabelë periodike me elementet, për shkak të rritjes së madhësisë së atomeve duke zbritur grupin. Shpjegim: Dhe kështu karakteri metalik i atomit rritet dhe prej andej bazueshmëria zvogëlohet
Si zvogëlohet NADP në reaksionin e varur nga drita?

Fotofosforilimi jo ciklik Elektronet nga PS I mund të kalojnë gjithashtu në një bartës elektroni dhe më pas të kombinohen me jonet e hidrogjenit (nga uji) për të reduktuar NADP në NADPH. Ky NADP i reduktuar përdoret në serinë e ardhshme të reagimeve
Kur vëllimi i një kampioni të gazit zvogëlohet presioni i mostrës së gazit?

Presioni në rënie Ligji i kombinuar i gazit thotë se presioni i një gazi lidhet në mënyrë të zhdrejtë me vëllimin dhe drejtpërdrejt me temperaturën. Nëse temperatura mbahet konstante, ekuacioni reduktohet në ligjin e Boyle. Prandaj, nëse ulni presionin e një sasie fikse gazi, vëllimi i tij do të rritet
Gjatë cilës ndarje zvogëlohet numri i kromozomeve në mejozë?
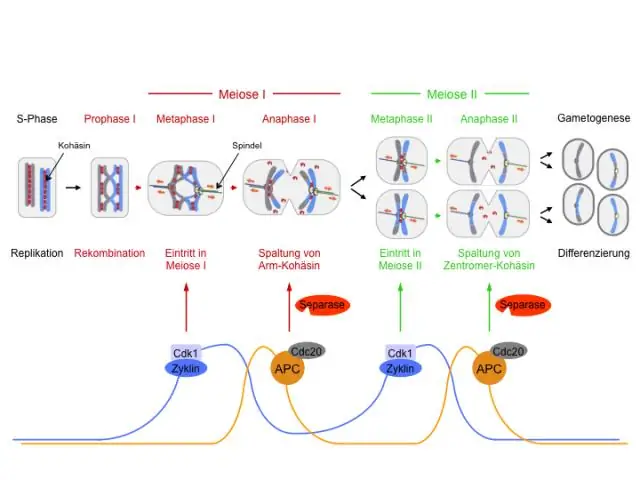
Ndarja e parë quhet ndarja e reduktimit - ose mejoza I - sepse zvogëlon numrin e kromozomeve nga 46 kromozome ose 2n në 23 kromozome ose n (n përshkruan një grup të vetëm kromozomesh)
Pse energjia e rrjetës zvogëlohet me madhësinë?

Ndërsa rrezja e joneve rritet, energjia e rrjetës zvogëlohet. Kjo është për shkak se me rritjen e madhësisë së joneve, distanca midis bërthamave të tyre rritet. Kështu, tërheqja midis tyre zvogëlohet dhe më në fund energjia e grilës më pak e çliruar gjatë procesit
