Përmbajtje:
- Autor Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:40.
- E modifikuara e fundit 2025-01-22 17:10.
Për të gjetur masën për qind përbërja e një elementi, pjesëtoni kontributin në masë të elementit me masën totale molekulare. Ky numër duhet të shumëzohet me 100% për t'u shprehur si a për qind.
Lidhur me këtë, si e gjeni përbërjen në përqindje?
Përbërja në përqindje
- Gjeni masën molare të të gjithë elementëve në përbërje në gram për mol.
- Gjeni masën molekulare të të gjithë përbërjes.
- Ndani masën molare të përbërësit me të gjithë masën molekulare.
- Tani do të keni një numër midis 0 dhe 1. Shumëzojeni atë me 100% për të marrë përbërjen e përqindjes.
Më pas, pyetja është, si e gjeni përqindjen e masës së një atomi? Hapi 1: Rendisni sasitë e njohura dhe të panjohura dhe planifikoni problemin. Ndryshoni secilën për qind bollëk në formë dhjetore duke e pjesëtuar me 100. Shumëzojeni këtë vlerë me masë atomike të atij izotopi. Shtoni së bashku për çdo izotop në marr mesatar masë atomike.
Gjithashtu pyetja është, si mund ta gjej përqindjen e një numri?
Nëse dëshironi e di sa për qind A është e B, thjesht pjesëtoni A me B, pastaj merrni atë numri dhe zhvendoseni vendin dhjetor dy hapësira djathtas. Kjo është e juaja përqindje ! Për të përdorur kalkulatorin, futni dy numrat për të llogaritur përqindje i pari është i dytë duke klikuar Llogarit Përqindje.
Cila është formula e molaritetit?
Formula e Molaritetit . Molariteti është termi më i përdorur për të përshkruar përqendrimin e një tretësire. Është e barabartë me molet e lëndës së tretur të ndarë me litra tretësirë. Lënda e tretur përkufizohet si substanca që tretet, ndërsa tretësi është substanca ku tretet substanca (zakonisht uji).
Recommended:
Si e llogaritni përqindjen e bollëkut të klorit?

Izotopi i klorit me 18 neutrone ka një bollëk prej 0,7577 dhe një numër masiv prej 35 amu. Për të llogaritur masën mesatare atomike, shumëzojeni thyesën me numrin masiv për secilin izotop, pastaj mblidhni ato së bashku
Si e gjeni përqindjen teorike të oksigjenit në KClO3?

Përqindja eksperimentale e oksigjenit në kampionin e KClO3 llogaritet duke përdorur këtë ekuacion. Eksperimentale % oksigjen = Masa e oksigjenit e humbur x 100 Masa e KClO3 Vlera teorike e % e oksigjenit në klorat kaliumi është llogaritur nga formula KClO3 me masë molare = 122,6 g/mol
Si e gjeni përqindjen e përafërt duke përdorur rregullin empirik?

Gjetja e zonës nën lakore nga x = 9 në x = 13. Rregulli empirik ose rregulli 68-95-99,7% jep përqindjen e përafërt të të dhënave që bien brenda një devijim standard (68%), dy devijime standarde (95%) , dhe tre devijime standarde (99.7%) të mesatares
Si e bëni përqindjen në Microsoft Word?
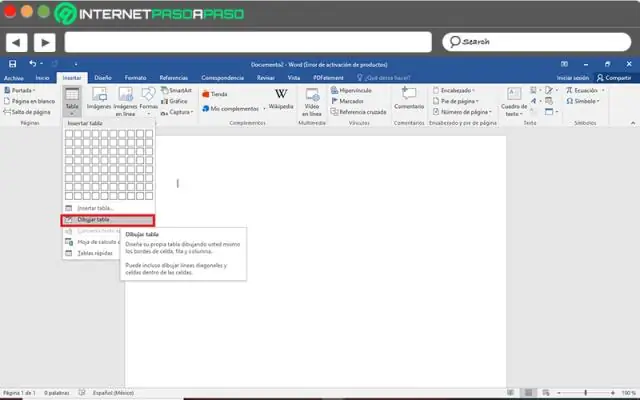
Shfaqni numrat si përqindje Zgjidhni qelizat që dëshironi të formatoni. Në skedën Home, në grupin Number, klikoni ikonën pranë Numrit për të shfaqur kutinë e dialogut Format Cells. Në kutinë e dialogut Format Cells, në Kategoritë, klikoni Përqindja
Si e llogaritni përqindjen e rënies së tensionit?

Për të llogaritur rënien e tensionit: Shumëzoni rrymën në amper me gjatësinë e qarkut në këmbë për të marrë amper-këmbë. Gjatësia e qarkut është distanca nga pika e origjinës deri në fundin e ngarkesës së qarkut. Pjestojeni me 100. Shumëzoni me vlerën e duhur të rënies së tensionit në tabela. Rezultati është rënia e tensionit
