
Përmbajtje:
- Autor Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:40.
- E modifikuara e fundit 2025-01-22 17:10.
Përbërja në përqindje sipas elementit
| Elementi | Simboli | Përqindja në masë |
|---|---|---|
| Hidrogjeni | H | 5.037% |
| Azoti | N | 34.998% |
| Oksigjen | O | 59.965% |
Thjesht kështu, sa është përqindja e masës së azotit në nh4no3?
Përgjigje dhe shpjegim: The përqindje në masë e nitrogjenit në nitratin e amonit mund të llogaritet me shprehjen siç tregohet më poshtë. Zëvendësoni vlerat e numrit të N - atomet, masa e N -atom, dhe masa e N H4 N O3 N H 4 N O 3 në ekuacionin e mësipërm. Prandaj, përqindje nga masë e azotit në nitratin e amonit është 34.999%.
Dikush mund të pyesë gjithashtu, sa azot ka në nitratin e amonit? Nitrat amonit është një pleh i rëndësishëm me vlerësimin NPK 34-0-0 (34% nitrogjenit ). Është më pak e përqendruar se urea (46-0-0), duke dhënë nitrati i amonit një disavantazh i lehtë i transportit.
Gjithashtu, si e llogaritni përqindjen në masë të azotit në nitratin e amonit?
Shpjegim:
- 2×14g=28g. Masa e N është 28 g. Përbërja në përqindje e N është 28g80g×100%=35%.
- 4×1g=4g. Masa e H është 4 g. Përbërja në përqindje e H është 4g80g×100%=5%.
- 3×16g=48g. Masa e O është 48 g. Përbërja në përqindje e O është 48g80g×100%=60%.
Cila është masa e formulës së nitratit të amonit?
80.043 g/mol
Recommended:
A është përzierja e klorurit të kaliumit me nitratin e natriumit një reaksion kimik?

Jo, nuk është sepse si kloruri i kaliumit ashtu edhe nitrat natriumi formojnë një tretësirë ujore, që do të thotë se ato janë të tretshme. Ato treten plotësisht në ujë, që do të thotë se nuk ka asnjë reaksion kimik të dukshëm në produkt. Kur përziejmë KCl me NaNO3, fitojmë KNo3 + NaCl. Ekuacioni jonik për këtë përzierje është
Cila është familja e azotit?

Grupi 15: Familja e Azotit. Familja e azotit përfshin komponimet e mëposhtme: azoti (N), fosfori (P), arseniku (As), antimoni (Sb) dhe bismuti (Bi). Të gjithë elementët e grupit 15 kanë konfigurimin e elektronevens2np3 në shtresën e tyre të jashtme, ku n është numri kuantik kryesor
Cila është ngarkesa formale e azotit në këtë strukturë?

Duke vazhduar me azotin, vërejmë se në (a) atomi i azotit ndan tre çifte lidhjesh dhe ka një çift të vetëm dhe ka gjithsej 5 elektrone valente. Ngarkesa formale në atomin e azotit është pra 5 - (2 + 6/2) = 0. Në (b), atomi i azotit ka një ngarkesë formale prej -1
Cili është ndryshimi midis masës së një protoni dhe masës së një elektroni?
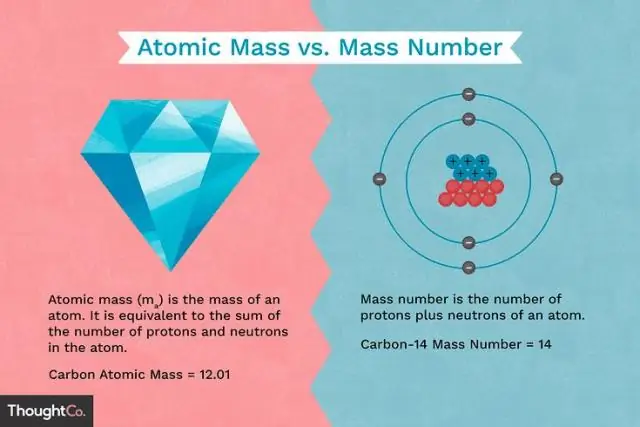
Protonet dhe neutronet kanë përafërsisht të njëjtën masë, por të dy janë shumë më masivë se elektronet (afërsisht 2000 herë më i madh se një elektron). Ngarkesa pozitive në një proton është e barabartë në madhësi me ngarkesën negative të një elektroni
Cili është ekuacioni jonik për nitratin e argjendit dhe klorurin e natriumit?

Për të shkruar ekuacionin jonik neto për AgNO3 + NaCl = AgCl + NaNO3 (nitrat argjendi + klorur natriumi) ndjekim tre hapat kryesorë
